

搜索
新冠感染防护用品准入
4月1日起中国出口新冠医疗物资须提供书面或电子声明
撰稿:lux更新日期:2020-10-29
2020年3月31日,中国国家商务部、海关总署、国家药品监督管理局联合发布有关有序开展医疗物资出口的2020年第5号公告,规定自2020年4月1日起,出口新型冠状病毒检测试剂、医用口罩、医用防护服、呼吸机、红外体温计的企业向海关报关时,须提供书面或电子声明(见下图),承诺出口产品已取得我国医疗器械产品注册证书,符合进口国(地区)的质量标准要求。海关凭药品监督管理部门批准的医疗器械产品注册证书验放。上述医疗物资出口质量监管措施将视疫情发展情况动态调整。
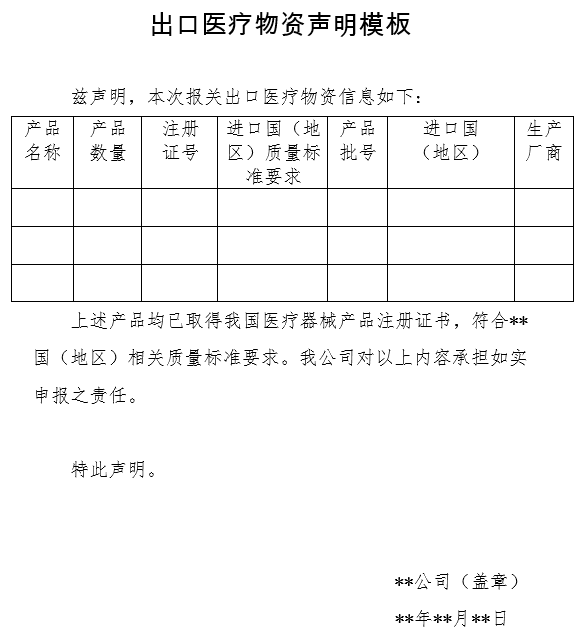
我国相关医疗器械产品注册信息(国家药监局网站www.nmpa.gov.cn动态更新)(以下链接列表信息截至2020.3.31):
http://images.mofcom.gov.cn/wms/202003/20200331221319022.xlsx
截至目前,国家药监局新型冠状病毒检测试剂注册信息有23条,国家及省级药监部门国产呼吸机注册信息62条,省级药监部门医用防护服注册信息301条,省级药监部门医用防护口罩注册信息150条,省级药监部门医用外科口罩注册信息523条,省级药监部门一次性使用医用口罩注册信息752条,省级药监部门红外体温计(含耳温计、额温枪)注册信息236条。
三部门强调,有关医疗物资出口企业要确保产品质量安全、符合相关标准要求,积极支持国际社会共同抗击疫情。



